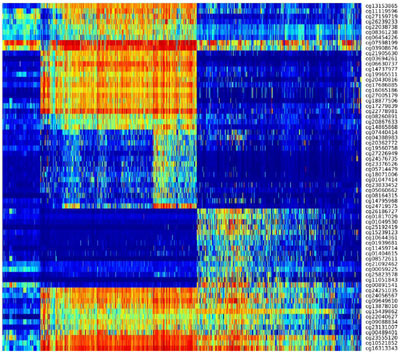
 Os cientistas analisaram 1.122 amostras de células e compararam esses dados aos resultados clínicos dos pacientes, o que levou à descoberta de novos indicadores moleculares para a caracterização desses tumores, o que permitirá prever com mais precisão o prognóstico dos pacientes.
Os cientistas analisaram 1.122 amostras de células e compararam esses dados aos resultados clínicos dos pacientes, o que levou à descoberta de novos indicadores moleculares para a caracterização desses tumores, o que permitirá prever com mais precisão o prognóstico dos pacientes.O artigo, intitulado Molecular profiling refines the classification of adult diffuse lower- and high-grade glioma (Perfis moleculares refinam a classificação de gliomas difusos de graus II, III e IV), apresenta sete subtipos para a avaliação da evolução desses tumores.
A classificação dos gliomas nos graus I, II, III ou IV, baseada no aspecto das células tumorais, está bem estabelecida e é adotada pela Organização Mundial de Saúde. Contudo, oncologistas observam que alguns pacientes com tumores considerados menos graves rapidamente sucumbem à doença enquanto outros com tumores classificados como mais agressivos sobrevivem por muitos anos.
Os achados do artigo explicam essa divergência, pois permitem a distinção mais precisa entre tumores, especialmente os de grau II ou III. Como os médicos usam esse diagnóstico para escolher o tipo e a intensidade do tratamento do paciente, a relativa falta de precisão no diagnóstico pode levar à prescrição terapêutica inadequada. Gliomas de graus II, III e IV são atualmente incuráveis. O tratamento alia cirurgia, quimioterapia e radioterapia.
“Estabelecemos o conjunto completo de genes associados a gliomas e usamos técnicas genômicas e moleculares para chegar a novos prognósticos”, afirma o professor da Faculdade de Medicina de Ribeirão Preto e coautor sênior do artigo, Houtan Noushmehr. “Descobrimos que gliomas classificados como de baixo ou de alto grau pertencem a subtipos diferentes. Essa foi uma descoberta inesperada e nos permitiu entender melhor a evolução dos gliomas quando separados de acordo com esses novos subtipos”, ressalta Noushmer.
O diretor da FMRP, Carlos Gilberto Carlotti, também participou do estudo. Para ele, o trabalho “é um ciclo completo” entre a clínica e a pesquisa fundamental. “A pesquisa partiu de uma pergunta clínica sobre como classificar melhor o tumor de um paciente e devolveu com a informação sobre alterações moleculares. Essa transferência do clínico para o pesquisador e do pesquisador para o clínico é extremamente importante”, avalia.
"Ao estudar a caracterização molecular, encontramos uma maneira muito mais precisa de predizer quais os tumores são mais propensos a crescer rapidamente. Isto permite prescrever os tratamentos de maneira mais adequada", explica o professor da Universidade de Columbia e outro co-autor sênior, Antonio Iavarone, cujo grupo fez a análise da expressão dos genes estudados e dos dados clínicos de pacientes.
"Esses resultados são um passo importante na compreensão dos gliomas como subconjuntos distintos de doenças e também dos mecanismos que levam à sua formação e evolução”, completa o professor associado da Universidade do Texas e terceiro co-autor sênior, Roel Verhaak.
O Centro de Câncer MD Anderson realizou a caracterização dos cromossomos das amostras.
Assessoria de Imprensa da USP



